元素周期表:https://ptable.com/?lang=zh-hans
化合价口诀:

元素、物质及微粒间的关系
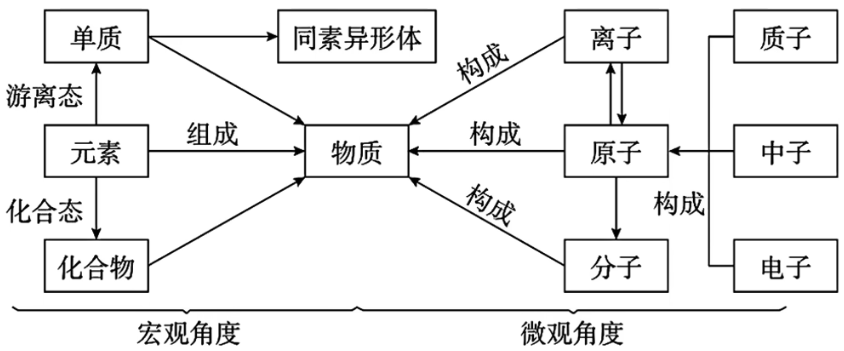
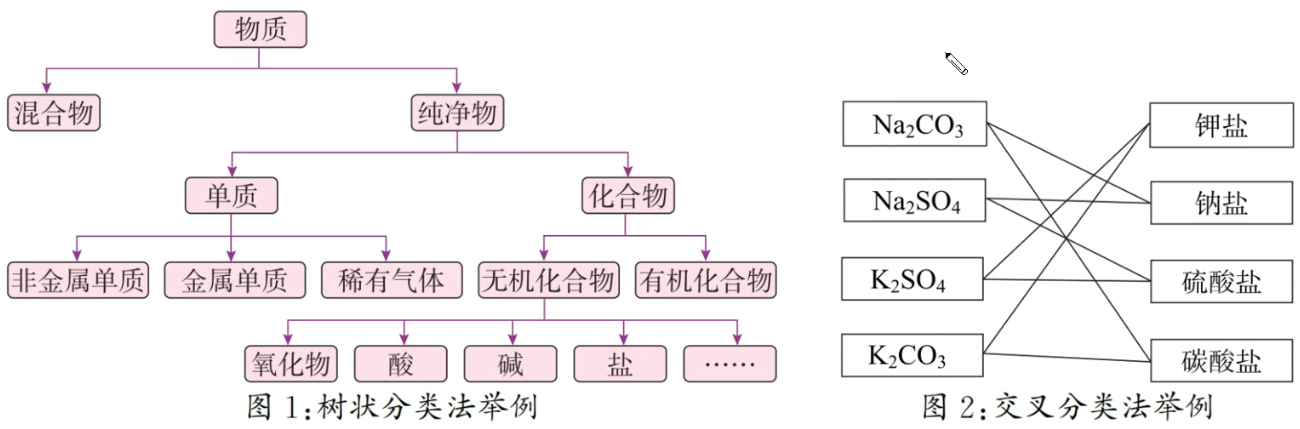
常见的分类方法:树状分类法、交叉分类法。
同素异形体
- 定义:由同种元素形成的不同性质的单质
- 对象:单质。
- 实例:金刚石、石墨、C6o;红磷、白磷;O2、O3。
注:
- 根据“结构决定性质”可知,同素异形体的性质不同,是因为单质分子的结构不同。
- 同素异形体相互转化属于化学变化。
- 只含一种元素的物质不一定是纯净物,如O2、O3的混合物。
氧化物:两种元素组成,其中一种元素为O
可分为:成盐(酸/碱/两性氧化物)和不成盐
化合价就是原子 “组队” 时的 “电子名额”—— 正价是 “给出名额”,负价是 “要取名额”,所有原子的名额加起来必须等于 0(化合物整体不带电),这样才能组成稳定的物质。
化学式中下方数字管 “一个分子 / 粒子里的原子数量”,左方数字管 “分子 / 粒子的整体个数”
酸性氧化物
(1)定义:能能与碱反应生成盐和水,且化合价不改变的氧化物
(2)常见物质种类:绝大多数非金属氧化物、部分金属氧化物。
(3)通性:
- 与碱反应生成盐和水,且化合价不变。
- 与碱性氧化物反应生成盐,且化合价不变。
- 若能与水反应,则生成对应价态的酸。
碱性氧化物
(1)定义:能与酸反应生成盐和水,且化合价不改变的氧化物。
(2)常见物质种类:绝大多数金属氧化物。
(3)通性:
- 与酸反应生成盐和水,且化合价不变。
- 与酸性氧化物反应生成盐,且化合价不变。
- 若能与水反应,则生成对应价态的碱。
h2so4 + naoh → na2so4 + h2o(酸 硫酸 + 碱 氢氧化钠 → 盐 硫酸钠 + 水)
两性氧化物
(1)定义:既能与酸反应转化为盐,又能与与碱反应转化为盐,且化合价均不改变的氧化物。
(2)常见物质种类:AlO3、ZnO、GazO3、BeO等。
(3)通性:酸性氧化物和碱性氧化物通性的总和。
电离就是电解质(如盐、酸、碱)溶解在水里或熔化时,拆成能自由移动的带电离子的过程。
判断氧化物是否为酸性氧化物的关键是看其是否存在等化合价的酸根。
干冰是固体形态的CO2,CO2是酸性氧化物;冰是固体形态的H2O,H2O不是酸性氧化物
食醋和稀硫酸都是溶液,溶液一定是混合物。醋酸化学式:CH3COOH
绝大多数金属氧化物都是碱性氧化物,Fe2O3和CuO是碱性氧化物